
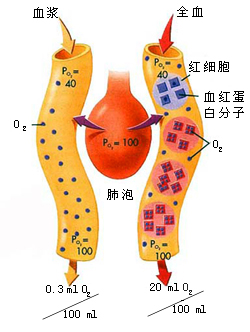
血液中物理溶解的O2量极少,不到血液总O2含量的1.0%,但它却是O2在血液运输过程中的重要环节。在假设温度和溶解度不变的情况下,O2的溶解量取决于PO2的大小,PO2高,溶解多;PO2低,溶解少。动脉血PO2是比较稳定的,一般是13.3 kPa(100 mmHg),在此PO2下每100 ml血液仅溶解0.3 ml O2。
O2的化学结合形式是HbO2,氧合血红蛋白。Hb是红细胞内的色蛋白,它的分子结构特征使之成为极好的运O2工具。Hb还参与CO2的运输,所以在血液气体运输方面Hb占有极为重要的地位。
每1个Hb分子由1个珠蛋白和4个血红素,又称亚铁原卟啉组成。每个血红素又由4个吡咯基组成一个环,中心是一Fe原子。每个珠蛋白有4条多肽链,每条多肽链与一个血红素相连接构成Hb的单体或亚单位。Hb是由4个单体构成的4聚体。Hb的4个单体之间和单体内部由盐键连接,Hb与O2的亲和力也随之改变,这是Hb氧离曲线呈S型和波尔效应的基础。
(1)Hb与O2的可逆结合:Hb和O2结合或离解是受PO2影响的,当PO2高时,Hb与O2结合成HbO2,而当PO2低时,HbO2则解离成Hb和O2,此反应不需酶催化,反应速度就很快,而且可逆。
(2)Hb与O2的结合反应是氧合而不是氧化:在此反应中,Fe2+与O2结合后仍是二价的铁,所以该反应是氧合,而不是氧化。而且只有在血红素的Fe2+与珠蛋白多肽链的组氨酸结合后,作用点才起作用,单独的血红素不是有效的O2载体。
(3)结合量:一分子Hb可以结合4分子O2,Hb分子量是64000~67000,所以1gHb可以结合1.34~1.39 ml O2,视Hb纯度而异。健康成人,如Hb的量为150 g/L,则1 L血液能结合O2的最大量约为200 m1。
血红蛋白氧容量:1L血液中Hb能结合O2的最大量。
血红蛋白氧含量:1L血液中Hb实际结合O2的量。
血红蛋白氧饱和度:血红蛋白氧含量 占血红蛋白氧容量的百分数。
在通常情况下,血中溶解的O2甚少,比起结合的O2可忽略不计。因此常常把血红蛋白氧容量叫做血氧容量(Oxygen Capacity),把血红蛋白氧含量叫做血氧含量(Oxygen Content),把血红蛋白氧饱和度叫做血氧饱和度(Oxyhemoglobin Saturation)。
HbO2呈鲜红色,氧离Hb呈紫蓝色。如果血液中含HbO2多,则血液呈鲜红色,如动脉血;如果血液中含氧离Hb多,则血液呈紫蓝色,如静脉血。假如毛细血管床血液中氧离Hb含量达50 g/L以上时,皮肤、粘膜呈紫蓝色,称为发绀。紫绀一般是HbO2减少;氧离Hb增加所造成。因此,紫绀一般是缺氧的标志。值得注意的是,有些严重贫血的病人,虽然存在缺O2,但由于Hb总量太少,以致毛细血管床血液中氧离Hb达不到50g/L故不出现紫绀;相反,有些患高原性红细胞增多症的人,虽然不存在缺O2,但因为Hb总量很多,以致毛细血管床血液中氧离Hb可达50g/L以上,而出现紫绀。此外,在CO中毒时,CO与Hb结合生成HbCO,呈樱桃红色。由于CO与Hb结合的能力是O2的210倍,故O2很难与Hb结合,造成缺O2。但此时氧离Hb并末增多,因此不出现紫绀,而呈现樱桃红色。
(4)Hb与O2的结合或解离曲线呈S型,与Hb的变构效应有关。目前认为Hb有两种构型:氧离Hb为T型,紧密型,氧合Hb为R型,疏松型。当O2与Hb的Fe2+结合后,Fe2+的电子自旋状态改变,原子半径变小,并移入卟啉环平面内, 盐键逐步断裂,Hb分子逐步由T型变为R型,对O2的亲和力逐步增加,R型的O2亲和力为T型的数百倍。也就是说,Hb4个亚单位无论在结合O2或释放O2时,彼此间有协同效应,即一个亚单位与O2结合后,由于变构效应的结果,其他亚单位更容易与O2结合;反之,当HbO2的一个亚单位释放出O2后,其他亚单位也更容易释放O2。因此,Hb氧离曲线呈S型。
氧离曲线(Oxygen-hemoglobin Dissociation Curve)表示PO2与Hb氧结合量或血氧饱和度关系的曲线。该曲线既表示不同PO2下,O2与Hb的分离情况,同样也反映不同PO2时,O2与Hb的结合情况。上面已提到曲线呈S型,是Hb变构效应所致。
(1)氧离曲线的上段:
相当于PO2为8~13.3kPa(60~100mmHg),即PO2较高的水平,因而认为PO2的变化对Hb氧饱和度影响不大。例如PO2为13.3kPa(100mmHg)时(相当动脉血PO2),血氧饱和度约为97.4%,氧含量约为194ml/L(19.4ml/dl);如将吸入气中PO2提高到20kPa(150mmHg),血氧饱和度为100%,只增加了2.6%,这就解释了为何VA/Q不匹配时,肺泡通气量的增加无助于O2的摄取;反之,如使PO2下降到9.3kPa(70mmHg),血氧饱和度为94%,也不过只降了3.4%。因此,即使吸入气或肺泡气PO2有所下降,如在高原、高空或某些呼吸系统疾病时,但只要PO2不低于8kPa(60mmHg),血氧饱和度仍能保持在90%以上,血液仍可携带足够的O2,不致于发生明显的低氧血症。
(2)氧离曲线的中段:
该段曲线较陡,相当于PO2为8~5.3kPa(60~40mmHg),是HbO2释放O2的部分。PO25.3kPa(40mmHg),相当于混合静脉血的PO2,此时血氧饱和度约为75%,氧含量约为144ml/L(14.4ml/dl),即每1L血液流过组织时释放了50mlO2。血液流经组织时释放出的O2容积所占动脉血氧含量的百分数称为O2的利用系数,安静时为25%左右。以心输出量5L计算,安静状态下人体每分钟耗O2量约为250ml。
(3)氧离曲线的下段:
该段相当于PO2为5.3-2kPa(40~15mmHg),也是HbO2与O2解离的部分,是曲线坡度最陡的一段,意即PO2稍降,HbO2就可大大下降。在组织活动加强时,PO2可降至2kPa(15mmHg),HbO2进一步解离,血氧饱和度降至更低水平,氧含量仅约44ml/L(4.4ml/dl),这样每1L血液能供给组织150ml O2,O2的利用系数提高到75%,是安静时的3倍。可见该段曲线代表O2储备。
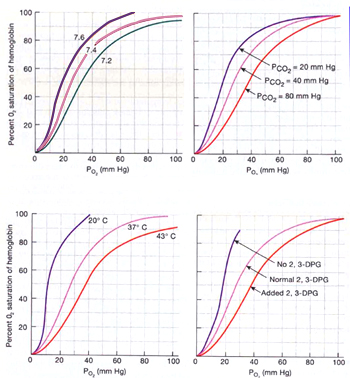
氧离曲线反映Hb和O2的亲和力的变化。通常用P50表示Hb对O2的亲和力。P50是使血氧饱和度达到50%时的PO2,正常为3.5kPa(26.5mmHg)。P50增大,表明Hb对O2的亲和力降低,需更高的PO2才能达到50%的血氧饱和度,曲线右移;P50降低,表示Hb对O2亲和力增加,达50%的血氧饱和度所需的PO2降低,曲线左移。影响Hb和O2亲和力或P50的因素有血液的pH、PCO2、温度和有机磷化物。
(1)pH和PCO2的影响:
血液[H+]和CO2增加均使氧离曲线右移,可解离更多的O2供组织利用。这与pH改变时Hb构型变化有关。酸度增加时,促使Hb分子构型变为T型,从而降低了对O2的亲和力,更易释放O2,曲线右移;酸度降低时,促使Hb变为R型,对O2的亲和力增加,曲线左移。酸度对Hb氧亲和力的这种影响,称为Bohr效应。Bohr效应的机制与pH改变时,Hb构型变化有关。酸度增加时,促使Hb变为T型,酸度降低时,促使Hb变为R型。PCO2的影响,一方面是通过PCO2改变时,pH也改变的间接效应,另一方面也通过CO2与Hb结合而直接影响Hb与O2的亲和力,不过后一效应极小。酸和CO2的影响效应有重要的生理意义,它有利于活动组织(酸性代谢产物与CO2增多)从血液中获得更多的O2,也有利于肺泡毛细血管中的Hb(排出CO2后)与O2结合。
(2)温度的影响:
温度升高(如在运动的肌肉中),曲线右移可解离更多的O2供组织利用。温度的影响可能与H+的活动度有关,即当温度升高时,H+的活动度增加,对Fe2+和O2结合的珠蛋白肽链分子构型变化的阻碍作用加强,使HbO2趋于解离。
(3)2,3-二磷酸甘油酸(2,3-DPG)的影响:
红细胞中含有多种有机磷化物,特别是2,3-DPG在调节Hb对O2的亲和力中起重要作用。2,3-DPG浓度升高,Hb对O2的亲和力降低,氧离曲线右移;2,3-DPG浓度降低,Hb对O2的亲和力增加,曲线左移。其机制可能是2,3-DPG与Hb的β链形成盐键,促使Hb变成T型的缘故。此外,2,3-DPG可能提高[H+],进而也可影响Hb对O2的亲和力。 2,3-DPG是红细胞无氧糖酵解的产物。用枸椽酸一葡萄糖液保存3周以上的血液,由于糖酵解停止,红细胞 2,3-DPG含量下降,Hb不易与O2解离。所以用大量贮存血液给病人输血,其运O2功能较差。
Hb不仅有运O2功能,还可缓冲组织氧分压,使组织氧分压不致因组织代谢水平的高低或外环境PO2的变动而发生很大的波动。
正常人在安静状态,组织平均需O2量是250ml/L,从氧离曲线可以看出,血液流经组织时PO2只需下降到5.3kPa(40mmHg)就可满足这一需氧量。所以组织正常PO2的上限应是5.3kPa(40mmHg),剧烈运动时, O2耗量增加,组织PO2只需略为下降,HbO2释放的O2量就可增加很多,因为这时是在氧离曲线很陡的下段。因此,组织PO2很少下降至2.6kPa(20mmHg)以下。可见虽然机体因活动强度的不同,需O2量随时有较大的变动,但是由于氧离曲线 的特性,保证组织内氧分压变动较小,仅在PO22.67~5.33kPa(20~40mmHg)范围内变动即可。
同时,组织的氧分压也不会因外环境的PO2大幅度的波动而发生很大的变化。例如在吸入高压O2时,即使高达66.67kPa (500mmHg),动脉血血氧饱和度最多也不过100%,比正常只增加3%,溶解的O2也只稍有增加。血液流经组织时,组织内的PO2也只是略有增加而已。其结果是,肺泡气PO2虽发生了较大变化,组织PO2的变动却很小。表明Hb不仅有结合和解离O2的功能,还有缓冲组织氧分压的功能。