
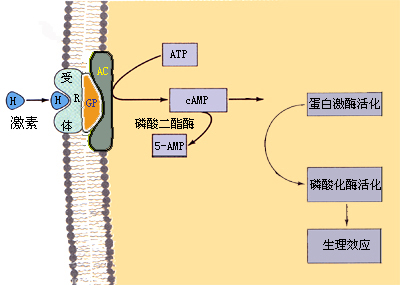
含氮激素作用于靶细胞膜上,与膜上的特异受体结合,从而激活膜上的腺苷酸环化酶(adenylate cyclase,AC),促进胞浆内三磷酸腺苷(ATP)转变为环一磷酸腺苷(cyclic AMP,cAMP), cAMP激活无活性的蛋白激酶, 通过催化细胞内蛋白质的磷酸化作用,诱发靶细胞的生理效应。在这一过程中,激素将信息传至靶细胞,而cAMP则将此信息传至细胞内的有关酶系, 因此称cAMP为第二信使,激素为第一信使。信息由第一信使传递给第二信使,引起细胞内一系列的酶促反应, 从而发生调节作用,这是第二信使学说的基本内容。
以cAMP为第二信使学说地提出,推动了激素作用机制的研究工作迅速深入发展。 近年来的研究资料表明,cAMP并不是惟一的第二信使,可能做为第二信使的化学物质还有cGMP、三磷酸肌醇、二磷酰甘油、Ca2+等。另外, 关于细胞表面受体调节、酰苷酸环化酶活化机制、蛋白激酶C的作用等方面的研究都取得了很大进展,现概述如下:
1.激素与受体的相互作用:激素的膜受体多为糖蛋白,其结构一般分为三部分:细胞膜外区段、质膜部分和细胞膜内区段。细胞膜外区段含有许多糖基,是识别激素并与之结合的部位。激素分子和靶细胞膜受体的表面,均由许多不对称的功能基团构成极为复杂而又可变的立体构型。激素和受体可以相从诱导而改变本身的构型以适应对方的构型,这就为激素与受体发生专一性结合提供了物质基础。
激素与受体的结合力称为亲和力(affinity)。一般来说, 由于相互结合是激素作用的第-步,所以亲和力与激素的生物学作用往往一致,但激素的类似物可与受体结合而不表现激素的作用,相反却阻断激素与受体相结合。实验证明,亲和力可以随生理条件的变化而发生改变,如动物性周期的不同阶段,卵巢颗粒细胞上的卵泡刺激素(FSH)受体的亲和力是不相同的。 某一激素与受体结合时,其邻近受体的亲和力也可出现增高或降低的现象。
受体除表现亲和力改变外,其数量也可发生变化。有人用人淋巴细胞膜上胰岛素受体进行观察发现,如长期使用大剂量的胰岛素,将出现胰岛素受体数量减少,亲和力也降低; 当把胰岛素的量降低后,受体的数量和亲和力可恢复正常。许多种激素(如促甲状腺激素、绒毛膜促性腺激素、黄体生成素、卵泡刺激素)都会出现上述情况。这种激素使其特异性受体数量减少的现象, 称为衰减调节或简称下调(down regulation)。下调发生的机制可能与激素-受体复合物内移入胞有关。相反, 有些激素(多在剂量较小时)也可使其特异性受体数量增多,称为上增调节或简称上调(up regulation),如催乳素、卵泡刺激素、血管紧张素等都可出现上调现象。下调或上调现象说明, 受体的合成与降解处于动态平衡之中,其数量是这一平衡的结果,它的多少与激素的量相适应,以调节靶细胞对激素的敏感性与反应强度。
2.G蛋白在信息传递中的作用 激素受体与腺苷酸环化酶是细胞膜上两类分开的蛋白质。激素—受体结合的部分在细胞膜的外表面,而腺苷酸环化酶在膜的胞浆面,两者之间存在一种起耦联作用的调节蛋白-鸟苷酸结合蛋白(guanine nucleotide-binding regulatory protein),简称G蛋白。G蛋白由α、β和γ三个亚单位组成,α亚单位上有鸟苷酸结合位点。当G蛋白上结合的鸟苷酸为GTP时则激活而发挥作用,但当G蛋白上的GTP水解为GDP时则失去活性。当激素与受体结合时,活化的受体便与G蛋白的α亚单位结合,并促使其与β、γ亚单位脱离,才能对腺苷酸环化酶起激活或抑制作用。
G蛋白可分为兴奋型G蛋白(Gs)和抑制型G蛋白(Gi)。Gs的作用是激活腺苷酸环化酶,从而使cAMP生成增多;Gi的作用则是抑制腺苷酸环化酶的活性,使cAMP生成减少。有人提出,细胞膜的激素受体也可分为兴奋型(Rs)与抑制型(Ri)两种,它们分别与兴奋性激素(Hs)或抑制性激素(Hi)发生结合,随后分别启动Gs或Gi,再通过激活或抑制腺苷酸环化酶使cAMP增加或减少而发挥作用。
3.三磷酸肌醇和二酰甘油为第二信使的信息传递系统 许多含氮激素是以cAMP为第二信使调节细胞功能活动的,但有些含氮激素的作用信息并不以cAMP为媒介进行传递,如胰岛素、催产紊、催乳素、某些下丘脑调节肽和生长因子等。实验表明,这些激素作用于膜受体后,往往引起细胞膜磷脂酰肌醇转变成为三磷酸肌醇(inositol 1,4,5-triphosphate,IP3)和二酰甘油(diacylglycerol,DG),并导致胞浆中Ca2+浓度增高。近年来,有人提出IP3和DG可能是第二信使的学说,引起人们的重视, 并且得到越来越多的实验证实。
这一学说认为,在激素的作用下,可能通过G蛋白的介导,激活细胞膜内的磷脂酶C(phospholipase C,PLC),它使由磷脂酰肌醇(PI)二次磷酸化生成的磷脂酰肌醇二磷酸(PIP2)分解,生成IP3和DG。DG生成后仍留在膜中,IP3则进入胞浆。在未受到激素作用时,细胞膜几乎不存在游离的DG,细胞内IP3的含量也极微, 只有在细胞受到相应激素作用时,才加速PIP2的降解,大量产生IP3和DG。IP3的作用是促使细胞内Ca2+贮存库释放Ca2+进入胞浆。细胞内Ca2+主要贮存在线粒体和内质网中。实验证明,IP3引起Ca2+的释放是来自内质网而不是线粒体,因为在内质网膜上有IP3受体,IP3与其特异性受体结合后,激活Ca2+通道,使Ca2+从内质网中进入胞浆。IP3诱发Ca2+动员的最初反应是引起短暂的内质网释放Ca2+,随后是由Ca2+释放诱发作用较长的细胞外Ca2+内流, 导致胞浆中Ca2+浓度增加。Ca2+与细胞内的钙调蛋白(calmodulin,CaM)结合后,可激活蛋白激酶,促进蛋白质磷酸化,从而调节细胞的功能活动。
DG的作用主要是它能特异性激活蛋白激酶C(protein kinase C,PKC),PKC的激活依赖Ca2+的存在。激活的PKC与PKA一样可使多种蛋白质或酶发生磷酸化反应,进而调节细胞的生物效应。 此外,DG的降解产物花生四烯酸是合成前列腺素的原料,花生四烯酸与前列腺素的过氧化物参与鸟苷酸环化酶的激活,促进cAMP的生成。cAMP作为另一种可能的第二信使,通过激活蛋白激酶G(PKG)而改变细胞的功能。
类固醇激素分子量小且是脂溶性的, 可以扩散通过细胞膜进入细胞内与胞浆中的受体结合,形成激素-胞浆受体复合物。激素-胞浆受体复合物可进入细胞核内。复合物再与核内受体结合, 转变为激素-核内受体复合物,启动DNA的转录过程,生成新的信使核糖核酸(mRNA)转移至胞浆内,翻译合成新的蛋白质(酶),从而引起相应的生理效应(见动画)。