
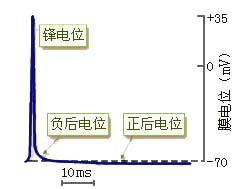
指膜受刺激后在原有的静息电位基础上发生的一次膜两侧电位的快速而可逆的倒转和复原。AP是由锋电位和后电位组成的。锋电位是AP的主要成分,因此通常说AP时主要指的是锋电位。 AP的幅度约为90~130mV,神经和骨骼肌纤维的AP的去极化上升支超过0mV电位水平约35mV,这一段称为超射。 神经纤维的AP一般历时0.5~2.0ms,可沿膜扩布,又称神经冲动(impulse)。因此,兴奋和神经冲动是动作电位的同意语。
由于AP的峰出现超射,即膜电位由静息时的内负外正转变成内正外负,Hodgkin认为:AP的形成可能不是单纯由于膜对K+通透性发生改变(如仅对K+不再通透,膜电位至多能达到零电位水平),而很可能是受刺激时膜对Na+产生通透的结果。他们降低细胞外液中的Na+浓度时,观察到AP峰电位的幅度和上升支的斜率均降低, 说明AP确是由于膜对Na+的通透性增加而造成的。而AP的复极化过程可能是由于膜重新对K+通透造成的。
(1)AP产生的离子学说:电压钳方法的研究
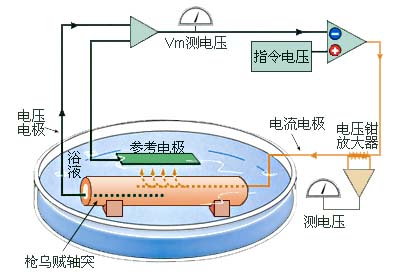
关于细胞受刺激时膜对Na+的通透性增加的原因,Hodgkin和Huxley认为, 可能是电刺激改变了膜的极化状态(膜电位改变),导致膜的通透性改变而出现离子流的结果。要证实这一猜想,只需人为改变膜电位的大小并观察其对离子流的影响。 然而,由欧姆定律可知,电阻一定时, 电流发生改变,必然引起膜电位随之变化,这样就无法观察膜电位对离子流的影响。于是他们创造性地设计并进行了著名的电压钳实验,通过将膜电位钳制在不同水平,以避免离子流反过来影响电压值。
电压钳方法:通过电压电极施加指令电压,若该电压变化引起了膜对Na+或K+的通透性发生改变,膜上将出现相应的离子流。电流电极记录到的膜电流值一方面作为实验结果,一方面又作为电压钳放大器发出的对抗电流的参考值,该对抗电流的大小与膜离子流相等,但方向相反,因而可维持指令电压。如果要单独观察Na+电流,可用TEA(tetraethylammonium,四乙基胺)阻断K+外流后得到;单独观察K+外流,则用TTX(tetrodotoxin,河豚毒)阻断Na+内流后得到。
压钳方法得到的结果:图表示膜去极化引起的电导(GNa和GK)的变化(是由钳制在指令电压V时,观察到的离子电流I,用欧姆定律计算出的)。
电导(G):G是电阻的倒数。 膜对某离子的电阻,是指膜对该离子通过的阻力大小,其倒数,G,则是该离子通过的容易程度,换句话说,也就是指通透性的大小。因此GNa和GK表示了Na+和K+的通透性。
可以看出:
①膜的GNa和GK都是电压依赖性的。去极化时,GNa和GK都增加,而且增加的幅度随去极化增加而加大;
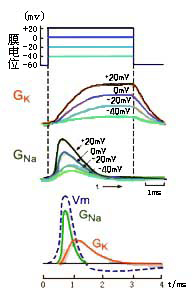
②去极化时,膜的GNa和GK变化的时程不同,GNa增加出现快,短时间内达到高峰,又很快下降;而GK则在去极化开始后延迟一段时间才缓慢增加,逐渐达到最大,只要去极化持续,就不会减弱,去极化结束后,再缓慢恢复。
从多次实验中,Huxley等得出了完满的数学模型。右下图的下图是他们用一次短暂的去极化刺激后引起的GNa和GK变化,和以其为基础重建(计算)的动作电位(虚线)。这种计算的动作电位与实验中记录到的几乎完全相同。
结论:动作电位的上升支(去极相)是因为膜对Na+的通透性增加导致的Na+内流引起的,而下降支(复极相)则是膜对K+的通透性增加导致的K+外流引起的。
(2)AP与电压门控离子通道:膜片钳方法的研究
膜片钳(patch clamp)技术:是将微电极尖端细胞膜上的单个离子通道的电流经高分辨放大后记录的技术。单个离子通道的电流(简称为单通道电流)是全或无的,电流很小,是pA级的。河豚毒和四乙基胺能单独阻断GNa和GK而不影响对方,同位素标记的两种毒素显示它们分别与细胞膜上不同的“点”特异结合。
这使人们推断细胞膜中有特殊的蛋白质离子通道的存在。而所谓膜对离子的通透性的改变,实际上是决定于这些离子通道蛋白质分子的功能状态。因此有必要对单个通道的特性进行研究。膜片钳技术在这样的研究背景下被催生出来。它通过与细胞膜接触的微电极尖端将一小片膜吸入尖端开口,并形成高阻封接,从而使这一小片膜与其余的细胞膜在电学上完全隔离开,这样就可对这一小片膜上的单个离子通道的电学特征进行研究。
膜片钳的研究结果:从图中可以看出,
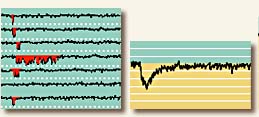
①通道的开放和关闭都是突然的,说明通道蛋白可以从一种构象快速跃变到另一种构象。
②通道开放时具有恒定的电导,即通道只有“开”或“关”两种状态,没有中间状态。
③同一个通道每次开放持续时间不一致,即通道开放的长短具有随机性。
④若化学门控通道结合了相应的信号分子,或电压门控通道处于特定的膜电位水平时,通道的开放几率增大。
膜片钳实验证明:不论是单个Na+通道电流或K+通道电流(B),将多次单个通道的电流总和后(C),与电压钳记录的全细胞膜(许多个)通道的电流(D)结果一致,进一步证明了细胞生物电现象的离子学说是正确的。
(3)电压门控离子通道的结构和性质:分子生物学方法的研究
离子通道蛋白质结构研究路线:用毒素(例如放射标记的TTX)与电压门控Na+通道结合→分离纯化并进行结构分析→得出分子结构→进行人工构建→膜片钳方法研究其功能特点→如构建的通道与毒素结合的通道功能相同,则证明结构分析是正确的。
通过上述方法准确揭示了电压门控Na+通道的分子结构 :它由2个α、β1和β2共4个亚基组成。α亚基上具有四个相似的结构域I,II,III,IV,它们可以围出一个中间孔道。每一个结构域又由六个α螺旋组成。目前认为,所有的电压门控离子通道可能属于同一个基因家族,因此在结构上是相似的。
(1)枪乌贼巨轴突膜上至少有两种电压门控的离子通道,即Na+通道和K+通道。它们各具有不同的功能状态。
电压门控Na+通道有两道门,三种功能状态。
关闭时,是备用状态,激活门关着,失活门开着;
激活时,是开放状态,两道门都开着;
失活时,是不能被激活的关闭状态,激活门开着,失活门关着。Na+通道被激活后必须首先进入失活状态,然后才能逐渐恢复到关闭状态以备下次被激活。Na+通道不可能直接由激活状态进入关闭状态。由于AP的产生是因Na+通道被激活导致Na+内流,所以Na+通道的状态必然影响细胞膜对新的刺激的反应性。当Na+通道进入失活状态时,无论给与细胞膜多么强的刺激,也不能诱发新的AP的产生,这就是绝对不应期。
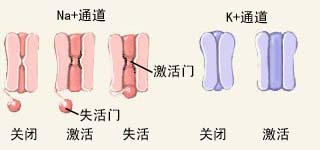
电压门控K+通道只有一道门,两种功能状态。安静时,是关闭状态,门是关着的;激活时,是开放状态,门是开着的
(2)AP的产生与离子通道的状态(AP产生原理的现代认识)
静息时,电压门控Na+通道和K+通道均处于关闭状态,而只有非门控K+通道开放并产生静息电位。
AP上升支的产生是因膜受刺激后,电压门控Na+通道开放,Na+迅速大量的内流导致膜发生去极化直至反极化。上升支的顶点接近于Na+平衡电位。
AP下降支的产生是因Na+通道开放后迅速失活,而K+通道延迟开放导致K+外流,细胞膜发生复极化。
后超极化期膜电位比RP值更负,这是因为细胞膜复极化到RP水平后,K+通道还未完全恢复到关闭状态,因而仍有少量的K+外流。
(3)AP(兴奋)后兴奋性变化的原理
锋电位期间细胞处于绝对不应期,此时任何强度的刺激均不能引起新的AP产生。 这是因为在AP的去极化相,Na+通道已全部打开。AP复极化相早期,即下降支的大部分时间内,Na+通道处于失活状态,此时Na+通道不可能再次被激活。
AP复极化的后期和后超极化期时,细胞处于相对不应期内,此时阈上刺激有可能引起AP的产生。原因是这时Na+通道部分恢复或完全恢复到关闭状态,可以接受刺激再次开放。但因K+通道仍然处于开放状态,K+外流可对抗Na+内流引起的去极化,所以必须有比阈刺激更强的刺激才能使膜电位去极化达到阈电位水平,而触发AP的产生。此时膜的兴奋性较正常时低。
(4)细胞内外的离子浓度不会因AP产生而改变
AP虽然是由Na+内流和K+外流产生的,但每次动作电位发生时跨膜的Na+、K+的量与细胞内外原有离子的量相比是很小的。枪乌贼巨轴突产生一次动作电位,膜内丧失的K+仅是原有K+的1/105,所以即使是短时间内产生多个AP,不至于使膜内外的离子浓度发生明显的改变。此外,钠泵的活动可因AP的出现而增强,从而维持细胞内外各种离子原有的浓度比。细胞内Na+增多或细胞外K+增多是引起钠泵活动加强的重要因素。 然而钠泵对离子的转运速度远比AP产生过程中离子的通透速度慢,因此短时间内的高频AP发生后,膜内外离子浓度梯度的完全恢复要相对滞后一些。